2020 官网升级中!现在您访问官网的浏览器设备分辨率宽度低于1280px请使用高分辨率宽度访问。
发布日期:2023-12-26
浏览次数:36
寒冬之下,现金流入、盈利是制药公司更愿意追求的确定性。无论是向机构融资,还是项目权益对外许可的首付款,又或者是创新药商业化的销售收入,都能为公司增加关系到“生存和发展”的资金弹药储备。相比融资和BD的不确定性,拥有商业化产品可以销售的公司能打的牌也更多一些,尤其是每年一度已经常态化的医保目录更新也给企业增加了更早更快释放商业潜力的确定性。
2023年医保谈判于近日落下帷幕,无论是总体谈判成功率(84.6%)还是1类创新药谈判成功率(92%),从2019年以来都在稳步上升,这也说明医保谈判规则的改善在结果上确实落在了实处,为创新药商业化增加了更多的确定性。亦有行业人士表示,医保制度的完善和平稳落地既鼓励了创新,又考虑到了医保基金的承受能力,正在无限接近那个微妙的平衡点。
作为23款谈判成功的1类创新药中的一分子,博锐生物自主研发和生产的首款国产CD20抗体药物泽贝妥单抗注射液(商品名:安瑞昔®)在上市的首年顺利被纳入了医保目录。这款药物成功进入医保对患者来说意味着什么?对博锐生物来说又意味着什么?医药魔方近日采访了博锐生物首席执行官(CEO)王海彬博士。

王海彬博士,浙江博锐生物制药有限公司CEO
从事微生物和生物制药领域研究与开发工作近30年,在该领域从早期开发到商业化生产均具有丰富经验,主导首款国产抗CD20抗体1类创新药和浙江省第一个融合蛋白以及第一个单抗上市。作为国家药典委员会委员、正高级工程师、中国药学会生物制品委员会委员和浙江省药学会生物制药专委会副主委,积极参与WHO关于生物类似药的技术指南制定,主持并圆满完成数十项国家和省部级项目,在国内外核心刊物发表论文近40篇,拥有PCT和国内发明专利数十项。曾获化工部科技进步一等奖、国家科技进步二等奖、国家八五科技攻关重大科技成果、浙江省药学会医药科技奖、浙江省科学技术二等奖、上海市科学技术二等奖、浙江省151人才工程重点培养人员、杭州市优秀企业家等殊荣,享国务院特殊津贴。
更早进入医保,优秀限度参与市场竞争
医保基金是我国医药市场优秀的支付主体,患者临床需求的满足主要依赖医保的支撑。进入医保目录意味着患者付费负担减轻,医院用药意愿加大,理论上自然会带动药品销量增长,对促进公司业绩增长的重要性也不言而喻。
“越早纳入医保,意味着越早进行广泛患者人群的渗透,让更多患者更早实现新药可及,减轻用药负担。同时让产品更大限度地参与市场竞争,获得销售回报助力企业下一轮研发,形成良性循环。”王海彬博士坦言:“这也是博锐生物在泽贝妥单抗上市的第一个年度就迅速推动其进入医保的动力。”
当然,也并不是说一款新药被纳入医保了就一定会获得丰厚的市场回报,其销售表现的好坏还是要看是否能够真正满足临床需求。
作为首款国产1类创新CD20抗体,泽贝妥单抗同样最早将目光聚焦在了血液瘤领域,首发获批并纳入医保的适应症为联合标准CHOP化疗治疗CD20阳性弥漫性大B细胞淋巴瘤(DLBCL)。这也是目前CD20抗体竞争最激烈的领域。那么,泽贝妥单抗又有哪些差异化优势有望助其在市场上夺得一席之地呢?
已上市CD20单抗[1]
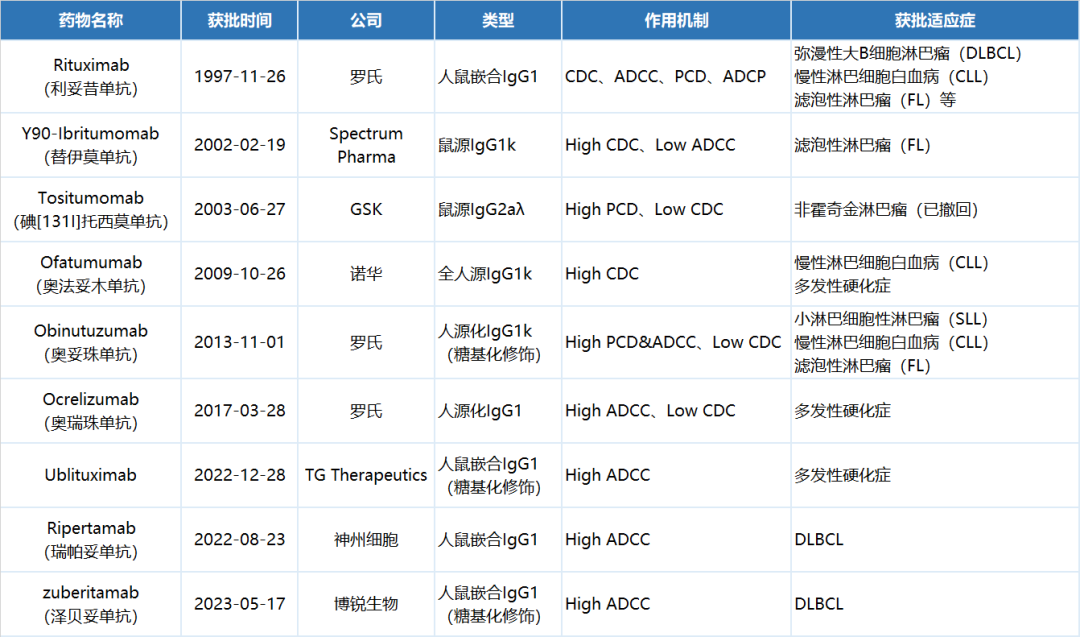
从分子设计上看。泽贝妥单抗是基于利妥昔单抗设计的一种新型人鼠嵌合型IgG1单抗,在抗体的互补决定区(CDR)进行了氨基酸的调整并减少抗体Fc片段的岩藻糖(Fucose)来增强它的ADCC效应。这个在临床前研究中得到了验证,泽贝妥单抗的ADCC效应相比利妥昔单抗提升了约10倍。结构的优化也带来了更高的组织穿透能力,泽贝妥单抗的II期PK数据显示,相比利妥昔单抗,其具有更高的分布容积。
增强的ADCC和更好的组织分布也让泽贝妥单抗在临床试验上取得了更优的无进展生存期(PFS)和总生存期(OS)数据。在泽贝妥单抗联合CHOP(Hi-CHOP)对比利妥昔单抗联合CHOP(R-CHOP)治疗DLBCL患者的III期研究中,Hi-CHOP组和R-CHOP组患者的ORR达到了非劣效性主要终点。对次要终点PFS和总生存期(OS)的分析显示,Hi-CHOP组的1年、2年、3年无进展生存率和总生存率均高于R-CHOP组。
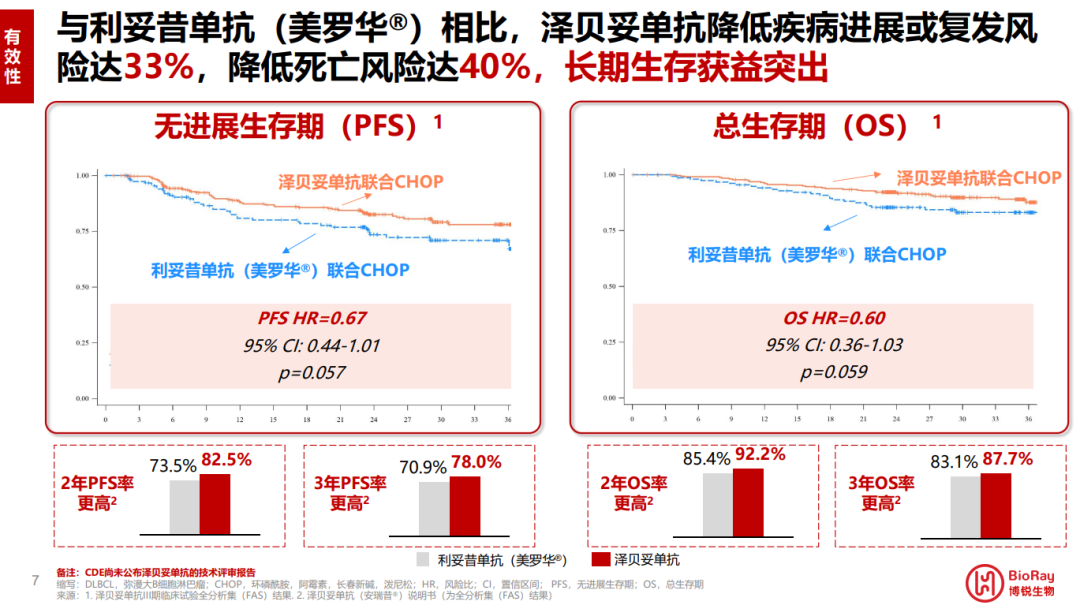
图源:参考资料[2]
DLBCL作为最常见的一种非霍奇金淋巴瘤(NHL)类型,约占NHL的30%~40%。据《中国淋巴瘤治疗指南2021版》报告,2020年中国NHL新发病例和死亡病例分别约为9.3万例和5.4万例。可靠的临床数据以及纳入医保带来的可及性提升意味着泽贝妥单抗将迎来更多医院覆盖。谈及接下来的工作安排时,王海彬博士表示:“安瑞昔®与CHOP联用的使用方式决定了安瑞昔®的使用场景多为住院病人,因此我们希望能够通过学术推广等方式,让更多医生及医疗机构了解到我们的产品价值以及为患者带来的获益,加快产品进院,让安瑞昔®惠及更多患者。”

稳定现金流保障,平稳穿越行业周期
当整个生物医药行业进入下行周期,很多公司为了“活下去”使出了浑身解数,转型做CDMO、压缩管线、售卖厂房裁员降本、对外授权……都成为企业自救手段。可以预见的是,“生存、过冬”仍会是许多Biotech未来一段时间面临的问题。
不过,这一挑战对于有稳定现金流预期的Biopharma博锐生物来说已经不足为惧。因为先做仿制药和生物类似药、后做创新药这种稳健的产品开发模式为博锐生物提供了安全的现金流保障,也为后续创新药的顺利开发奠定了坚实的基础。
生物类似药的开发周期相对较短、成功率更高,能尽快实现商业化变现,有利于公司的持续发展且更符合中国当时的国情,博锐生物深谙此道。如今,凭借4款自免领域的生物类似药/仿制药产品安佰诺(注射用重组人II型肿瘤坏死因子受体-抗体融合蛋白)、安佰特(英夫利西单抗生物类似药)、安健宁(阿达木单抗生物类似药)和安舒正(枸橼酸托法替布片),2022年博锐生物的自免领域销售额国内 。
博锐生物的第二款商业化产品安健宁在国内的销售额已经与原研产品修美乐(艾伯维)不相上下。2021年销售额合计约为4.6亿元,2022年营收超9亿元,是目前国产阿达木单抗销售业绩最高的产品。安佰特也有着不俗的销售表现,国内医院终端销售收入占比也仅次于原研产品类克(强生)。
各企业阿达木单抗国内医院终端销售收入占比
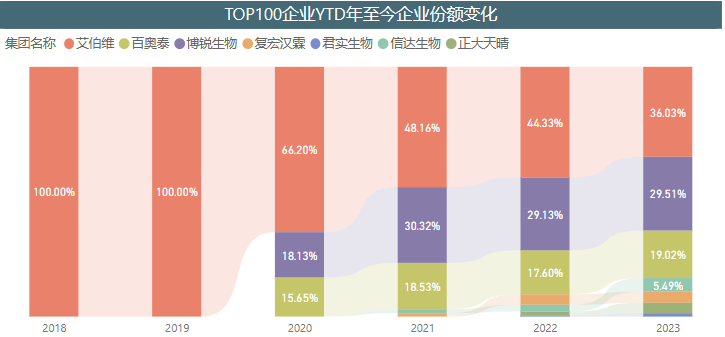
图源:医药魔方PharmaBI数据库
这几款产品的商业化推广过程同时也使博锐生物锻造了一支非常优秀的商业化团队,助力公司销售收入在过去三年取得超50%的复合年增长率。加上今年肿瘤领域两款新产品安瑞泽®(注射用曲妥珠单抗)和泽贝妥单抗的上市,博锐生物迎来“六安时代”,其商业化品种的销售已经形成一定规模,在市场竞争力上不容小觑。
这样的局面得益于博锐生物坚定清晰地执行战略规划,脚踏实地、有条不紊地向目标平稳推进而不被外界干扰。王海彬博士也将此视为 “博锐人”应对行业寒冬的态度。“首先,要坚定想法,经过内部讨论和打磨过后,就不能轻易改变战略上的定位;其次,要把事情实实在在做好,博锐的团队一直以来都比较稳定,大家都在踏踏实实地做事,慢慢形成了行业里的一道风景线。”
向“自免+肿瘤免疫”双龙头迈进
“苟”过资本寒冬对于很多Biotech来说算是当下第一要务,不过对于博锐生物来说,这家已经实现研发、生产、销售端到端全面布局的Biopharma已经将目光瞄向了更远的未来——向“自免+肿瘤免疫”双龙头迈进。博锐生物正在持续深耕以探索更多创新药物,拥抱新疗法,并搭建了拥有20+款产品的在研管线。
在肿瘤免疫领域,博锐生物目前拥有10多款在研产品,靶点涵盖肿瘤免疫过程中的多个生物标志物,涉及单抗、双抗、三抗和ADC等多种药物类型以期服务更多的患者群体。
两款三特异性抗体BR110和BR115分别被开发用于治疗血液瘤和实体瘤,研发进度全球起先。BR110引进自恩沐生物,是全球第一个获批临床的抗CD3/CD19/CD20三抗产品,目前正在国内开展治疗复发/难治性(R/R) CD20和/或CD19 阳性B细胞血液恶性肿瘤患者,已于今年9月完成首例患者给药,BR110有望解决单一靶点靶向治疗后的耐药性问题。
BR115靶向CD3/HER2/HER2的1类创新型生物制品,具有更好的肿瘤特异性,并且可以更好地针对TAA突变引起的肿瘤逃逸,该款候选药物目前也已申报临床。
ADC药物市场规模在近几年正以双位数的增速不断扩大,2023年有望突破100亿美元大关。这类药物巨大的商业前景也成为各大企业布局的重点。自2022年以来,ADC相关交易并购持续火热。仅2023年,国内实现出海项目TOP15中,ADC占多半(8/15)。艾伯维、阿斯利康、辉瑞、GSK、BMS等巨头重金布局。
博锐生物则差异化布局了靶向LIV-1(ZIP6)的ADC新药BRY812,是国内第一个、全球第二个获批临床的LIV-1 ADC,目前已完成I期临床首例受试者给药。
在自身免疫领域,博锐生物已有比较扎实的研发经验,除了4款已上市产品外,第7款药物托珠单抗注射液生物类似药(商品名:安佰欣)的上市申请也于2023年2月7日获CDE受理。5月24日,BR201注射液获批临床实验申请,伴随着这些产品的加持,博锐生物在自免领域的优势地位也将随之进一步提升。
博锐的雄心还不止于此,创新药国际化愿景在其首款SIRPα单抗成功获FDA批准临床中迈出了踏实的一步。王海彬博士表示,目前的I期研究将由公司自己推进,等到进入II期阶段,看到一些好的数据后,会考虑与美国本土的一些企业合作。
“2023年以来,博锐生物获得2个产品上市批准、2个报产申请、3个IND批准和2个完成I期首例患者给药、1个产品临床试验申请美国FDA批准。博锐生物在不断前进着。我们从创新1.0走向创新2.0+的飞跃,完成了产品1.0矩阵的布局及创新药全球化战略布局的有序推进,也正式开启了双免领域新篇章。同时,我们也通过对外合作引进,自身创新研发,拥抱新兴疗法,差异化布局新靶点、新适应症,且成功实现6款产品上市,这些都将帮助博锐生物更好的走出差异化路线。”王海彬博士最后补充道。
总结
虽说行业尚处于“寒冬”之际,不过,我们也在这一过程中看到了中国制药企业综合实力的显著提升。整个行业也都在求新、求变中不断进化、成长。博锐生物就是其中一个典型的例子。从数款生物类似药成功上市,到首款创新药泽贝妥单抗十年磨一剑的成功研发上市,再到此次顺利纳入医保……每每坚实的一小步也都汇成了博锐生物发展长河中的见证。前路漫漫亦灿灿,期待中国更多生物医药公司的崛起。
参考文献:
[1]The applications of anti-CD20 antibodies to treat various B cells disorders.
[2]YPSW202300066-W1(ppt).pdf (nhsa.gov.cn)

回到顶部