2020 官网升级中!现在您访问官网的浏览器设备分辨率宽度低于1280px请使用高分辨率宽度访问。
发布日期:2021-12-31
浏览次数:88
自1986年美国FDA批准第一款治疗性单克隆抗体药物上市以来,全球已累计超100款抗体药物上市。经过短短30几年的发展,以单抗为主要代表的抗体类药物已经革新了包括自身免疫性疾病、癌症在内的多种疾病的治疗。在市场表现方面,阿达木单抗蝉联药王宝座多年,2020年单药年销售额高达198亿美元;同年,位列全球畅销药TOP10的4种单抗累计销售额近500亿美元。
除了获批数量的飞速增长以及市场规模的急剧扩大,过去30多年,在技术迭代方面,抗体类药物也有了重要突破。其中,以双特异性抗体和三特异性抗体为代表的多特异性抗体已成为抗体领域的后起之秀。以双特异性抗体为例,自2014年以来,美国FDA已累计批准3款产品(blinatumomab、emicizumab、amivantamab)上市,为急性淋巴细胞白血病、A型血友病以及转移性非小细胞肺癌患者带来了新的治疗选择。
在双特异性抗体接连取得研发突破,且形成了全球超500个项目同步在研的竞争浪潮的同时,三特异性抗体的研发序幕也已悄然拉开。
三特异性抗体是指特异性结合至3个抗原并包含三个或更多个抗原结合域的分子。来自全球多家机构的药物研发人员正在全力开发这类分子,希望发挥三特异性抗体同时调控多个靶点的优势,为癌症、自身免疫性疾病、HIV感染等疾病提供更有效的疗法。
据医药魔方NextPharma数据库,目前全球有超过30款三特异性抗体候选分子在研,其中三成以上的项目已处于临床开发阶段,包括赛诺菲CD28/HER2/CD3三抗SAR443216、CD38/CD28/CD3三抗SAR442257 、anti-HIV三抗SAR441236;Harpoon的HPN536 (MSLN/CD3/albumin三抗)、HPN217(CD3/albumin/BCMA三抗)、HPN823(CD3/DLL3/albumin三抗);Numab/基石药业的三抗ND021(PDL1/albumin/4-1BB)等。
表1 部分处于临床开发阶段的三抗
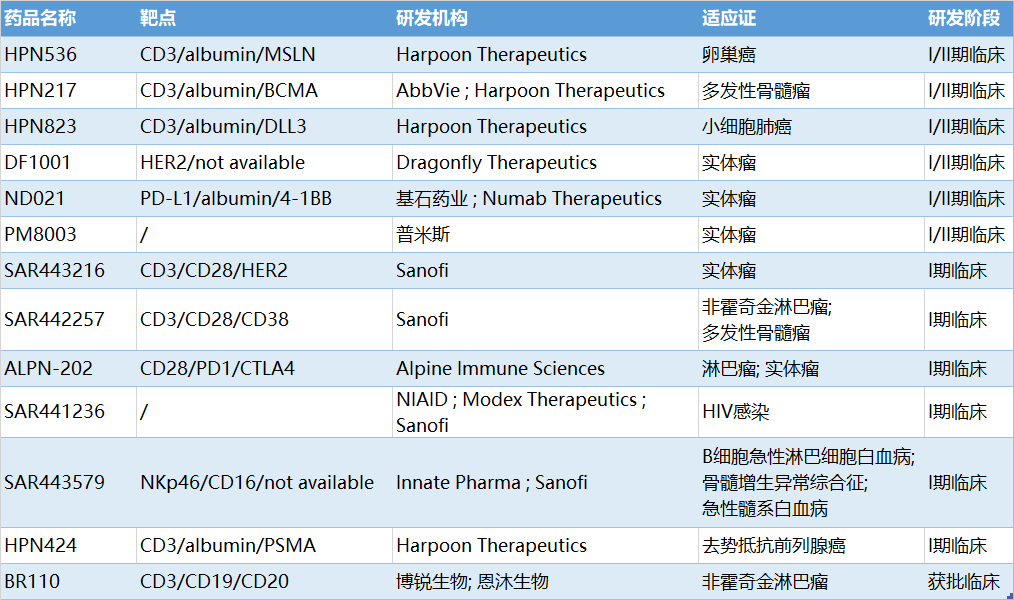
来源:NextPharma数据库
过去几年,国内有多家企业加入了三特异性抗体研发的第一波浪潮,如恩沐生物、普米斯、基石药业、道尔生物、盛诺基、嘉和生物等。其中,深耕双抗和三抗领域,已建立具有自主知识产权的双抗DICAD及三抗TRIAD平台的恩沐生物于12月29日公布了研发里程碑,公司靶向CD3/CD19/CD20的三特异性抗体BR110(CMG1A46)的临床试验申请已获得国家药品监督管理局(NMPA)批准。据悉,这是全球首个获批临床的抗CD3/CD19/CD20三抗产品。
同一天,恩沐生物同时宣布与专注于免疫领域的创新型生物制药企业博锐生物达成了合作协议,博锐生物作为独家合作伙伴获得了恩沐生物靶向CD3/CD19/CD20的三特异性抗体BR110(CMG1A46)在大中华地区(包括中国大陆、香港、澳门及台湾)的临床开发、生产及商业化权益。

博锐生物CEO王海彬博士:“新药研发虽不是易事,但做成的成就感、荣誉感难以言喻。”
三抗开发靶点选择五花八门,博锐生物/恩沐生物为何选择开发CD3/CD19/CD20三抗?相比同行,恩沐生物的三抗TRIAD平台有何独特的优势?BR110(CMG1A46)的临床前研究数据如何?未来前景如何?近日,医药魔方就这些问题采访了博锐生物CEO王海彬博士。
全球首个:CD3/CD19/CD20三抗临床获批
据王海彬博士介绍,BR110是恩沐生物基于其全球 的自主研发三特异性抗体TRIAD技术平台开发的一款151 KD的IgG样“ 1:(1 + 1)”三特异性抗体。BR110(CMG1A46)能够同时靶向T细胞表面的CD3和肿瘤细胞上的两个不同抗原CD20和CD19,通过拉近肿瘤细胞和T细胞的空间距离,激活T细胞,杀伤表达CD19和/或CD20的肿瘤细胞。
去年12月,在ASH年会上,恩沐生物公布了BR110(CMG1A46)治疗非霍奇金淋巴瘤(NHL)的临床前研究数据。根据大会摘要,由于BR110(CMG1A46)与肿瘤细胞表面的CD19和CD20都具有很高的亲和力,因此它不仅可以靶向CD19+/CD20+DLBCL细胞,还可以针对CD19-/CD20+DLBCL细胞,以及CD20低表达的DLBCL细胞。
体外研究中,BR110(CMG1A46)能够以剂量依赖性方式通过人外周血单个核细胞(PBMC)介导肿瘤细胞裂解。与基于IgG形式的常规“1:1”CD3xCD20双特异性抗体相比,CMG1A46显示出更强的效力和安全性。此外,研究还显示,在同时表达CD19和CD20的细胞,以及仅表达CD19或CD20的细胞中,BR110(CMG1A46)均能诱导有效的肿瘤裂解。
体内研究显示,在移植了人类PBMC的NOD小鼠模中,BR110(CMG1A46)显示出了强大的肿瘤抑制活性,并诱导了CD19+/CD20+Jeko-1淋巴瘤和CD19+/CD20- A20-hCD19肿瘤的快速消退。
在食蟹猴中的药代动力学研究表明,以1mpk(mg/kg)剂量给药时,BR110(CMG1A46)在血清中的半衰期超过70小时。给药剂量高达10mpk(mg/kg)时也未导致显著的不良反应。首次给药后24小时内,CMG1A46可使外周血中的B细胞被迅速完全消除。完成最后一次给药后(1mpk),外周B细胞消除可持续至少28天。
总结来说,在体外和体内实验中,BR110(CMG1A46)表现出比传统的“1:1”IgG格式的其他CD3xCD20双特异性抗体更好的效力和安全性。在食蟹猴中的初步研究显示,BR110(CMG1A46)在血清中具有天然IgG样半衰期,且毒性可控。这些数据表明,作为一种新型的CD19/CD20靶向T细胞衔接三特异性抗体,BR110(CMG1A46)具有非常好的抗肿瘤潜力,临床开发前景令人期待。
此次IND申请获批不仅是BR110迈向临床开发阶段的关键里程碑,也是对恩沐生物三特异性抗体TRIAD技术平台成药性的重要验证,同时也代表了国产三特异性抗体开发的又一突破。
王海彬博士告诉医药魔方:“抗体类药物的开发,包括双抗和三抗,如果分子更接近人体天然IgG的结构,那么它的安全性会更高,免疫原性会更低。恩沐生物的双抗和多抗的平台开发出的分子正是如此,药代特性好,半衰期长,CMC与传统单抗几乎无差异。此外,恩沐生物的DICAD/TRIAD平台可开发1:1:1、1:2、2:2、1:1等多种类价数,灵活度非常高,这对于后续其它不同类型候选分子的开发非常关键。因此,除了就BR110的开发达成合作,博锐生物还获得了利用恩沐生物自主研发的DICAD/TRIAD双/多特异性抗体平台开发多个双/多特异抗体资产的独家授权。我们相信,这无疑将为博锐生物在双抗/多抗领域的进一步扩展奠定坚实基础。”
一箭双雕:三特异性抗体独具优势
靶向CD19、CD20等B细胞抗原的疗法是B细胞恶性肿瘤患者的重要临床治疗手段,如CD20单抗、CD19 CAR-T细胞疗法。然而,很多患者会在接受治疗后因靶点表达下调或丢失,导致疾病复发。
举例来说,CD20单抗是目前治疗B细胞恶性肿瘤的最重要治疗方案。然而,有1%-2%的B细胞淋巴瘤患者为CD20阴性。此外,已有多项研究报道,在R-CHOP方案(CD20单抗利妥昔单抗+环磷酰胺+多柔比星+长春新碱+泼尼松龙)治疗后复发/进展的CD20阳性(+)弥漫性大B细胞淋巴瘤(DLBCL)患者中,有20%以上的患者出现CD20表达下调的现象。
此外,尽管CD19 CAR-T细胞疗法是B细胞恶性肿瘤患者一种突破性免疫治疗途径,但对于侵袭性B细胞非霍奇金淋巴瘤(NHL)来说,只有30%-40%的患者在使用CD19 CAR-T细胞产品治疗后可保持长期的无进展生存,大多数患者要么不响应CD19 CAR-T细胞疗法,要么在最初响应后病情会复发。一种常见的复发机制是,癌细胞上CD19抗原下调,出现CD19阴性克隆。接受CD19 CAR-T细胞疗法治疗后复发的B细胞NHL患者的活检显示,大约30%的患者肿瘤为CD19阴性。
为了解决单一靶向疗法因靶点丢失或下调导致的耐药难题,降低抗原阴性克隆逃逸介导的复发风险,同时靶向多个B细胞抗原被提出作为一种治疗策略,如已经有临床数据公布的CD20xCD19双靶点CAR-T,以及正在迈向临床开发的CD3/CD19/CD20三特异性抗体等。
在CD20xCD19双靶点CAR-T开发方面,来自全球的多个研究团队已经公布了积极的临床结果。2020年10月,来自美国威斯康星医学院的一个研究团队报道了在复发B细胞恶性肿瘤患者中调查CD20xCD19双靶点CAR-T细胞疗法的首个I期试验(NCT03019055)的结果。研究显示,输注新鲜生产的CD20xCD19双靶点CAR-T细胞表现出了良好的安全性、较低的毒性以及较高的疗效(第28天ORR为100%,CRR达92%)。今年7月,解放军总医院韩为东主任团队在Leukemia杂志上公布了利用其自主研发的CD20xCD19双靶点CAR-T细胞治疗复发/难治性非霍奇金淋巴瘤(r/rNHL)患者的I/II期临床研究长期随访数据:87例患者,最佳ORR为78% (95% confidence interval [CI], 68–86),其中70%的患者达到完全缓解;中位随访27.7个月,中位无进展生存期达27.6个月。
CD3/CD19/CD20三特异性抗体的开发与CD20xCD19双靶点CAR-T有着相同的科学基础,同时也具有自身独特的优势。
“与CD20xCD19双靶点CAR-T一样,我们的三特异性抗体BR110的开发也是选择靶向CD19和CD20这两种肿瘤抗原,CD19和CD20都是淋巴瘤中经过验证的成熟靶点,均有相应的靶向疗法获批上市。CD20xCD19双靶点CAR-T披露的积极早期临床数据也为同时靶向肿瘤中的这两个抗原提供了初步概念验证。而相比双靶点CAR-T,我们的三特异性抗体BR110还具有多方面的潜在优势,一方面,已有的实验数据表明,BR110对CAR-T耐药样本仍然有效;另一方面,由于BR110的结构与天然IgG的结构非常接近,具有良好的CMC成药性,因此与必须个性化定制的自体CAR-T疗法相比,在大规模生产方面具有很大的优势,随之而来就是药价的大幅降低。可以说,三抗就像是‘通用型’的CAR-T,因此非常有希望为B细胞恶性肿瘤患者带来更加安全、有效的创新疗法。”王海彬博士解释道。
最终理想:免疫领域龙头BioPharma
王海彬博士是生物医药领域的领军人物,拥有近30年生物制药领域研发、临床、生产和项目管理经验,带领团队研发出一款又一款新药,给无数患者带来了福音。自2019年出任博锐生物总裁以来,带领公司聚焦免疫领域这一黄金赛道,围绕自身免疫和肿瘤免疫开展创新生物药研发。目前博锐生物已拥有超过10个处于不同研发阶段的产品管线。
在自身免疫领域,博锐生物以“四安”(安佰诺®、安健宁®、安舒正®、安佰特®)为产品主线覆盖风湿科、皮肤科、消化科等主要科室,并积极布局其他管线(包括针对前瞻性靶点的分子),持续夯实其在自免领域的 地位。在肿瘤免疫领域,博锐生物以细胞类型覆盖为靶点布局主线,以肿瘤微环境下的不同免疫细胞机制为产品布局策略,全方位打造多款肿瘤免疫管线。单抗开发方面,CD73单抗已获批临床,SIRPα单抗分子专利已公开;双抗/三抗开发方面,除了IND申请刚刚获批的三特异性抗体BR110,此前,博锐生物已经申请一款PD-L1/TGF-β双抗专利,并获得临床批件。此外,博锐生物同时也在开发多款抗体偶联药物(ADC)。
王海彬博士告诉医药魔方,经过多年的积淀,博锐生物已经在抗体类药物开发方面形成了巨大的优势。从生物学机制的理解,到靶点的选择、临床前候选化合物(PCC)的开发;从细胞株的构建,到上下游工艺的开发,公司建立了完备的抗体药物研发综合体系。除了高效开发传统单抗,这套体系也将成为双抗、三抗等创新疗法的研发“加速器”。
谈及博锐生物未来3-5年的规划,王海彬博士强调了三个关键词:创新、两步走、临床导向。
--创新
王海彬博士强调,目前在新药研发领域,信息全球同步化,竞争亦是如此。如何在全球化的竞争环境中走向金字塔的顶端,创新不可或缺。过去2年多,博锐生物在创新方面进行了大量投入,除搭建了丰富的创新生物药管线,还在美国圣地亚哥也成立了一家创新公司,且在上海筹建了一个新的研发基地。公司希望,这些前期投入在接下来的5-10年里能够转化为自身免疫以及肿瘤免疫领域的best-in-class疗法,惠及国内外患者。
--两步走
未来几年,在拓展创新药管线方面,博锐生物将采用in house+license in两步走的策略。在积极内部自研的同时,也会根据公司的战略需求,适时引进外部项目。
--临床导向
对于是否会布局目前生物医药研发领域非常热门的细胞疗法、基因疗法、RNA疗法等方向,王海彬博士指出,博锐生物的研发始终以临床需求为导向,不会盲目地跟风“热点”。未来,如果在博锐生物所聚焦的自身免疫和肿瘤免疫领域,有疾病需要用到创新技术去攻克,那么公司会考虑进行相应的布局。
采访的最后,王海彬博士表示,传统Pharma创新化,Biotech“Pharma化”是国内医药行业发展的大势。对于很多传统Pharma来说,不创新将可能被时代淘汰,对新兴的Biotech来说,搭建闭环的研-产-销体系才能更具全球竞争力。可以预见的是,未来,行业里会有越来越多兼具创新、生产、销售能力的BioPharma诞生。作为一家已搭建丰富管线、重视创新的公司,博锐生物希望能够发展为一家全球知名的免疫领域龙头BioPharma。
参考资料:
[1] 176 Preclinical Study of a Novel Tri-Specific Anti-CD3/CD19/CD20 T Cell-Engaging Antibody As a Potentially Better Treatment for NHL(来源:ASH官网)
[2] I期数据积极!双特异性CAR-T疗法:高效抗肿瘤,ORR达82% | Nature子刊 (来源:医药魔方Pro)
[3] Nirav N. Shah et al. Bispecific anti-CD20, anti-CD19 CAR T cells for relapsed B cell malignancies: a phase 1 dose escalation and expansion trial. Nature Medicine(2020).
[4] Yajing Zhang et al. Long-term activity of tandem CD19/CD20 CAR therapy in refractory/relapsed B-cell lymphoma: a single-arm, phase 1–2 trial. Leukemia (2021)
[5] 2020年全球药品销售额TOP100(来源:医药魔方Info)

回到顶部