2020 官网升级中!现在您访问官网的浏览器设备分辨率宽度低于1280px请使用高分辨率宽度访问。
发布日期:2021-12-29
浏览次数:53
2021年12月29日,博锐生物与恩沐生物共同宣布, BR110(CMG1A46)CD3/CD19/CD20三特异性抗体临床试验申请于今日获得国家药品监督管理局(NMPA)批准,这是全球首个进入临床的抗CD3/CD19/CD20三抗产品,博锐生物享有大中华区权益。
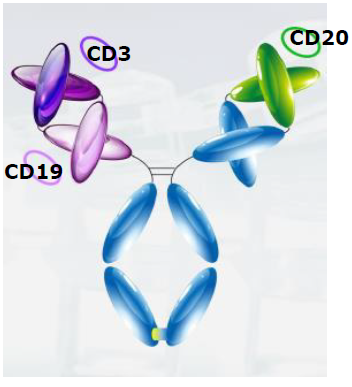
罗氏、Xencor等发现CD3/TAA双抗中,肿瘤相关抗原arm与CD3 arm的价态比对于抗肿瘤活性和安全性至关重要。基于相关研究,罗氏和Xencor分别开发了2:1 TCB技术平台和2+1 XmAb双抗技术平台,TAA抗体:CD3抗体的比例都为2:1。
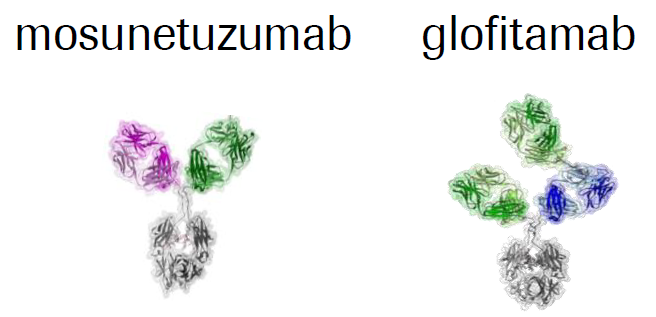
BR110的CD3/CD19/CD20三抗中,CD19和CD20为肿瘤相关抗原,因此TAA:CD3也为2:1。所不同处,BR110中TAA包括CD19和CD20。CD19、CD20都是淋巴瘤中经过验证的成熟靶点,CD3双抗和CAR-T都取得优异临床数据,而CD19/CD20双特异性抗体的早期临床数据表现出比CD19 CAR-T更好的有效性和安全性。
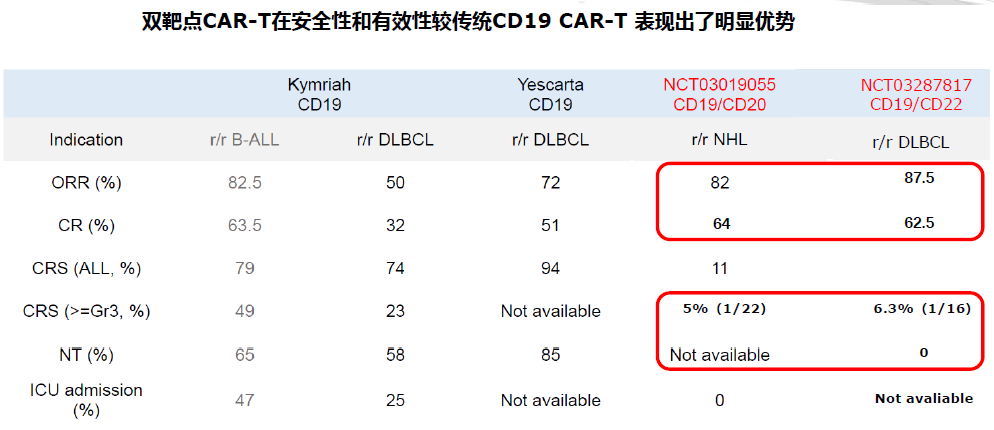
基于上述结果发现,BR110该三抗分子相当于整合了2:1 TCB双抗和CD19/CD20双靶点的协同效应,有望成为同类最优药物。
2021年10月4日,强生与Xencor达成合作协议,以12亿美元引进后者的CD3/CD20双抗和CD28双抗。其中CD3/CD20双抗的重要拓展方向即为与CD19抗体的联合治疗。
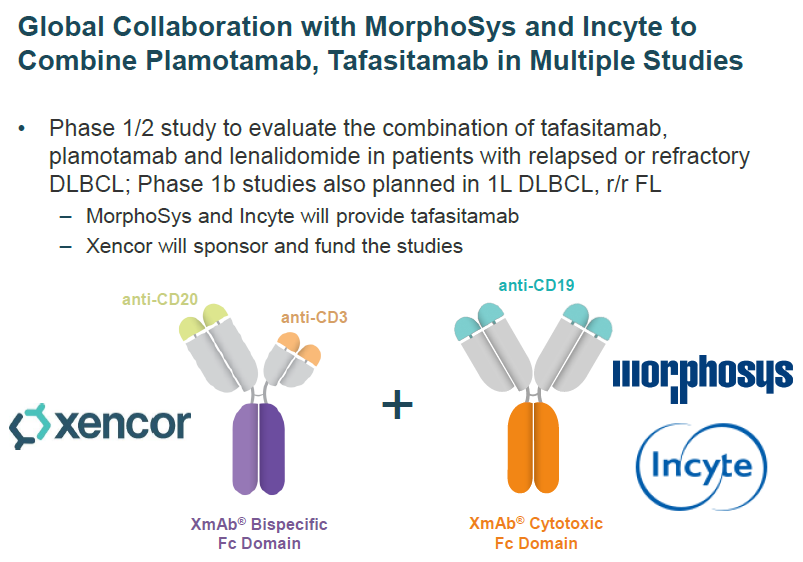
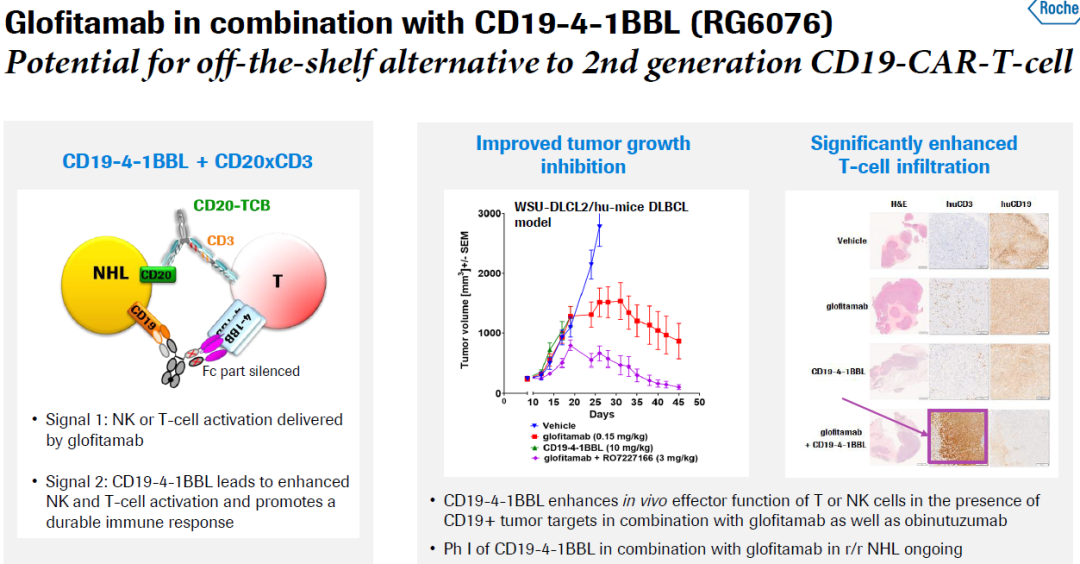
罗氏则在探索CD3/CD20双抗Glofitamab与CD19/4-1BBL抗体融合蛋白联用,寄希望于替代CD19 CAR-T疗法。
诺诚健华与康诺亚联合开发CD3/CD20双抗,同时引进Incyte的CD19单抗,其拓展方向可能也是两者的联用。相比于强生、罗氏、诺诚健华的双抗+单抗联用,BR110的CD3/CD19/CD20可能会起到同样的协同作用,作为单药给药则更加方便。
总结
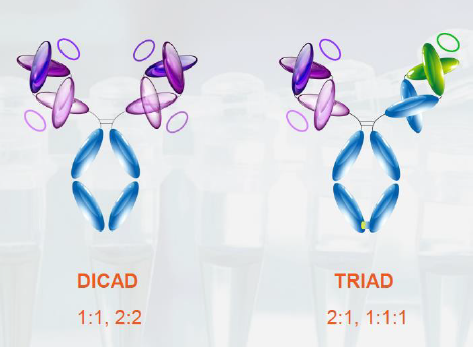
博锐生物已经建立了丰富的研发管线,广泛覆盖肿瘤免疫和自身免疫等领域。博锐生物已有4款上市药物,分别为阿达木单抗类似药-安健宁®、依那西普类似药-安佰诺®、英夫利西单抗类似药-安佰特®和枸橼酸托法替布片-安舒正®。创新药方面,博锐生物已经申报了PD-L1抗体、CD73抗体、CD20抗体、SIRPa抗体和PD-L1/TGFβ双抗,后续研发管线还包括多个ADC、双抗、免疫检验点抗体和Th2、Th17通路的自身免疫抗体新药等。此次与恩沐生物的合作,进一步扩充了博锐生物的研发管线,DICAD/TRIAD技术平台也将为博锐生物在双抗/多抗领域的进一步扩展提供坚实基础。

回到顶部